膜片钳技术的基本原理是通过负反馈使得膜电位与指令电压相等,在电压钳制的条件下记录膜电流。上面是电阻反馈式膜片钳放大器的电路示意图。A1为一极高输入阻抗、极低噪声的场效应管运算放大器,由于A1极高的开环增益使得两个输入端的电压几乎完全相等,使用膜片钳全细胞记录技术观察拮抗剂对烟碱受体激动剂量效曲线的影响,从而实现电压钳制。Rf为一数值可切换的反馈电阻,分别对应于不同的电流记录范围,其中高值反馈电阻具有极高的电阻和极低的杂散电容,是决定放大器单通道记录性能的基本元件。膜片钳使用操作流程及注意事项:凡是在本平台使用仪器的同学必须履行实验室相关要求。合肥全自动膜片钳成像

膜片钳使用的注意事项:工作原理膜片钳是一种能够直接观察单一的离子通道蛋白质分子对相应离子通透难易程度等特性的一种实验技术。它的基本原理是以一个光洁,直径约为0.5~3um的玻璃微电极同神经或肌细胞的膜接触,之后对微电极另一端开口处施加适当的负压用电极的纤细开口将与电极接触的那一小片膜轻度吸入,如此在微电极开口处的玻璃边沿以及这一小片膜周边会形成紧密的封接,它的电阻能够达到数个或数十个千兆欧,这世界上就是在化学上完全隔离了吸附在微电极开口处的那一片膜同膜的其余部分,通过微电极记录到的电流变化光光和该膜片中通道分子的功能状态相关联。合肥全自动膜片钳成像膜片破裂再将玻管慢慢地从细胞表面垂直地提起,断端游离部分自行融合成脂质双层。
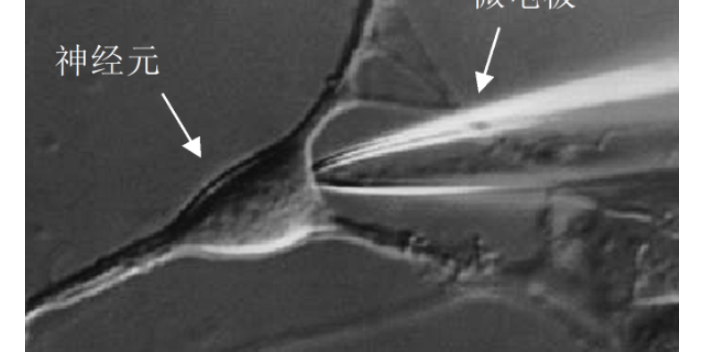
膜片钳的数据如何处理:穿孔膜片(perforated patch)是为克服常规全细胞模式的胞质渗漏问题,有学者将与离子亲和的制霉菌素或二性霉素b经微电极灌流到含有类甾醇的细胞膜上,形成只允许一价离子通过的孔,用此法在膜片上做很多导电性孔道,借此对全细胞膜电流进行记录。由于此模式的胞质渗漏极为缓慢,局部串联阻抗较常规全细胞模式高,所以钳制速度很慢,也称为缓慢全细胞模式。它适合于小细胞的电压钳位,对于直径大于30μm的细胞很难实现钳位。不足之处是由于电极与细胞间交换快,细胞内环境很容易破坏,因此记录所用的电极液应与胞浆主要成分相同,如高k+,低na+和ca2+及一定的缓冲成分和能量代谢所需的物质。膜片钳技术用特制的玻璃微吸管吸附于细胞表面,使之形成10~100MΩ的高阻封接,被孤立的小膜片面积为微米数量级,因此封接范围内细胞膜光有少数离子通道。
全细胞膜片钳模式下有电压钳记录和电流钳记录两种。电压钳记录的原理与电压钳技术相似,但有所不同:首先,全细胞电压钳记录只使用单根电极,但在电学效果上同时实现了电压钳制和电流记录。其次,电压钳记录的电极不细胞,对细胞造成的损伤较小,因而能用于小细胞如神经元的研究。电流钳记录则是通过钳制电极电流来测量膜电位。电流钳在本质上也是电压钳位,它将差分放大器的输出电流与指令电流相比较,然后将这个差动输出施加到放大器前级的倒相端,通过高速反馈使得同相端的电压与其相等,无论电极电流是否为零,都能从输出电压得到膜电位的准确数值。膜片钳技术用于纪录全细胞或个别细胞膜上离子信道电生理特性的研究方法。
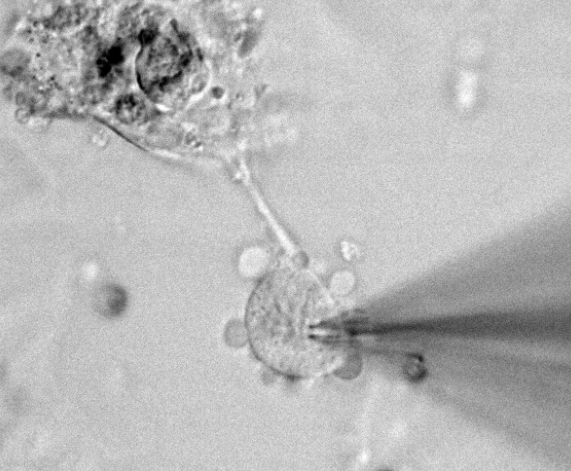
膜片钳系统有如下应用局限性(1)光能应用于悬浮细胞的纪录,因此大部分的纪录对象为化细胞,而对于需要贴壁生长的大多数正常细胞,现有的自动膜片钳系统就无法纪录;(2)在纪录对象上,目前的膜片钳系统只能纪录胞膜形状平整饱满的细胞,大部分是工具细胞如化细胞,此类细胞有比较强的细胞膜可以禁得起各种人为操作,而许多具有研究价值的细胞(例如元代培养的神经元)胞膜较弱容易破裂,且胞体表面不规整,现有的自动膜片钳系统难以派上用场。因此,迫切需要一种新型的全自动膜片钳电生理纪录系统来解决以上问题。用膜片钳技术可以直接观察和分辨单离子通道电流及其开闭时程。合肥全自动膜片钳成像
膜片钳使用操作流程及注意事项:电热加热线温度很高,在使用时注意避免烫伤。合肥全自动膜片钳成像
膜片钳操作实验:膜片钳放大器是整个实验系统中的中心,它可用来作单通道或全细胞记录,其工作模式可以是电压钳,也可以是电流钳。从原理来说,膜片钳放大器的探头电路即I-V变换器有两种基本结构形式,即电阻反馈式和电容反馈式,前者是一种典型的结构,后者因用反馈电容取代了反馈电阻,降低了噪声,所以特别适合很低噪声的单通道记录。由于供膜片钳实验的专门计算机硬件及相应的软件程序的相继出现,使得膜片钳实验操作简便、效率提高。如与EPC-9型膜片钳放大器(内含ITC-16数据采集/接口卡)配套使用的软件PULSE/PULSEFIT,它既可产生刺激波形,控制数据采集,又可分析数据,同时具有用于膜电容监测的锁相放大器,多种软件功能集成于一体。合肥全自动膜片钳成像